Электролиз расплавов и растворов. Подготовка выпускников к ЕГЭ. "Тема электролиза в ЕГЭ" Задание егэ химия электролиз
Электролиз расплавов и растворов (солей, щелочей)
Если в раствор или расплав электролита опустить электроды и пропустить постоянный электрический ток, то ионы будут двигаться направленно: катионы к катоду (отрицательно заряженному электроду), анионы к аноду (положительно заряженному электроду).
На катоде катионы принимают электроны и восстанавливаются, на аноде анионы отдают электроны и окисляются. Этот процесс называют электролизом.
Электролиз — это окислительно-восстановительный процесс, протекающий на электродах при прохождении электрического тока через расплав или раствор электролита.
Электролиз расплавленных солей
Рассмотрим процесс электролиза расплава хлорида натрия. В расплаве идет процесс термической диссоциации:
$NaCl→Na^{+}+Cl^{-}.$
Под действием электрического тока катионы $Na^{+}$ движутся к катоду и принимают от него электроны:
$Na^{+}+ē→{Na}↖{0}$ (восстановление).
Анионы $Cl^{-}$ движутся к аноду и отдают электроны:
$2Cl^{-}-2ē→{Cl_2}↖{0}$ (окисление).
Суммарное уравнение процессов:
$Na^{+}+ē→{Na}↖{0}|2$
$2Cl^{-}-2ē→{Cl_2}↖{0}|1$
$2Na^{+}+2Cl^{-}=2{Na}↖{0}+{Cl_2}↖{0}$
$2NaCl{→}↖{\text"электролиз"}2Na+Cl_2$
На катоде образуется металлический натрий, на аноде — газообразный хлор.
Главное, что вы должны помнить: в процессе электролиза за счет электрической энергии осуществляется химическая реакция, которая самопроизвольно идти не может.
Электролиз водных растворов электролитов
Более сложный случай — электролиз растворов электролитов.
В растворе соли, кроме ионов металла и кислотного остатка, присутствуют молекулы воды. Поэтому при рассмотрении процессов на электродах необходимо учитывать их участие в электролизе.
Для определения продуктов электролиза водных растворов электролитов существуют следующие правила:
1. Процесс на катоде зависит не от материала, из которого сделан катод, а от положения металла (катиона электролита) в электрохимическом ряду напряжений, при этом если:
1.1. Катион электролита расположен в ряду напряжений в начале ряда по $Al$ включительно, то на катоде идет процесс восстановления воды (выделяется водород $Н_2$). Катионы металла не восстанавливаются, они остаются в растворе.
1.2. Катион электролита находится в ряду напряжений между алюминием и водородом, то на катоде восстанавливаются одновременно и ионы металла, и молекулы воды.
1.3. Катион электролита находится в ряду напряжений после водорода, то на катоде восстанавливаются катионы металла.
1.4. В растворе содержатся катионы разных металлов, то сначала восстанавливается катион металла, стоящий в ряду напряжений правее.
Катодные процессы
2. Процесс на аноде зависит от материала анода и от природы аниона.
Анодные процессы
2.1. Если анод растворяется (железо, цинк, медь, серебро и все металлы, которые окисляются в процессе электролиза), то окисляется металл анода, несмотря на природу аниона.
2.2. Если анод не растворяется (его называют инертным — графит, золото, платина), то:
а) при электролизе растворов солей бескислородных кислот (кроме фторидов ) на аноде идет процесс окисления аниона;
б) при электролизе растворов солей кислородсодержащих кислот и фторидов на аноде идет процесс окисления воды (выделяется $О_2$). Анионы не окисляются, они остаются в растворе;
в) анионы по их способности окисляться располагаются в следующем порядке:
Попробуем применить эти правила в конкретных ситуациях.
Рассмотрим электролиз раствора хлорида натрия в случае, если анод нерастворимый и если анод растворимый.
1) Анод нерастворимый (например, графитовый).
В растворе идет процесс электролитической диссоциации:

Суммарное уравнение:
$2H_2O+2Cl^{-}=H_2+Cl_2+2OH^{-}$.
Учитывая присутствие ионов $Na^{+}$ в растворе, составляем молекулярное уравнение:
2) Анод растворимый (например, медный):
$NaCl=Na^{+}+Cl^{-}$.
Если анод растворимый, то металл анода будет окисляться:
$Cu^{0}-2ē=Cu^{2+}$.
Катионы $Cu^{2+}$ в ряду напряжений стоят после ($Н^{+}$), по этому они и будут восстанавливаться на катоде.

Концентрация $NaCl$ в растворе не меняется.
Рассмотрим электролиз раствора сульфата меди (II) на нерастворимом аноде :

$Cu^{2+}+2ē=Cu^{0}|2$
$2H_2O-4ē=O_2+4H^{+}|1$
Суммарное ионное уравнение:
$2Cu^{2+}+2H_2O=2Cu^{0}+O_2+4H^{+}$
Суммарное молекулярное уравнение с учетом присутствия анионов $SO_4^{2-}$ в растворе:

Рассмотрим электролиз раствора гидроксида калия на нерастворимом аноде:

$2H_2O+2ē=H_2+2OH^{-}|2$
$4OH^{-}-4ē=O_2+2H_2O|1$
Суммарное ионное уравнение:
$4H_2O+4OH^{-}=2H_2+4OH^{-}+O_2+2H_2O$
Суммарное молекулярное уравнение:
$2H_2O{→}↖{\text"электролиз"}2H_2+O_2$
В данном случае, оказывается, идет только электролиз воды. Аналогичный результат получим и в случае электролиза растворов $H_2SO_4, NaNO_3, K_2SO_4$ и др.
Электролиз расплавов и растворов веществ широко используется в промышленности:
- Для получения металлов (алюминий, магний, натрий, кадмий получают только электролизом).
- Для получения водорода, галогенов, щелочей.
- Для очистки металлов — рафинирования (очистку меди, никеля, свинца проводят электрохимическим методом).
- Для защиты металлов от коррозии (хрома, никеля, меди, серебра, золота) — гальваностегия.
- Для получения металлических копий, пластинок — гальванопластика.
Тема 6. «Электролиз растворов и расплавов солей»
1. Электролиз – окислительно – восстановительный процесс, протекающий на электродах при пропускании электрического тока через раствор или расплав электролита.
2. Катод – отрицательнозаряженный электрод. Происходит восстановление катионов металлов и водорода (в кислотах) или молекул воды.
3. Анод – положительнозаряженный электрод. Происходит окисление анионов кислотного остатка и гироксогруппы (в щелочах).
4. При электролизе раствора соли в реакционной смеси присутствует вода. Поскольку вода может проявлять и окислительные и восстановительные свойства, то она является «конкурентом» и для катодных и для анодных процессов.
5. Различают электролиз с инертными электродами (графитовые, угольные, платиновые) и активным анодом (растворимым), а также электролиз расплавов и растворов электролитов.
КАТОДНЫЕ ПРОЦЕССЫ
Если металл находится в ряду напряжений:
Положение металла в ряду напряжений
Восстановление на катоде
от Li до Al
Восстанавливаются молекулы воды: 2H2O + 2e- → H20+ 2OH-
от Mn до Pb
Восстанавливаются и молекулы воды и катионы металла:
2H2O + 2e- → H20+ 2OH-
Men+ + ne- → Me0
от Сu до Au
Восстанавливаются катионы металлов: Men+ + ne- → Me0
АНОДНЫЕ ПРОЦЕССЫ
Кислотный остаток
Асm-
Анод
Растворимый
(железо, цинк, медь, серебро)
Нерастворимый
(графит, золото, платина)
Бескислородный
Окисление металла анода
М0 – nе- = Mn+
анод раствор
Окисление аниона (кроме F-)
Асm- - me- = Ас0
Кислородсодержащий
Фторид – ион (F-)
В кислотной и нейтральной средах:
2 H2O - 4e- → О20 + 4H+
В щелочной среде:
4ОН- - 4е- = О20+ 2Н2O
Примеры процессов электролиза расплавов с инертными электродами
В расплаве электролита присутствуют только его ионы, поэтому на катоде восстанавливаются катионы электролита, а на аноде окисляются анионы.
1. Рассмотрим электролиз расплава хлорида калия.
Термическая диссоциация КСl → K+ + Cl-
К(-) К+ + 1e- → K0
А (+) 2Сl- - 2e- → Cl02
Cуммарное уравнение:
2КСl → 2K0 + Cl20
2. Рассмотрим электролиз расплава хлорида кальция.
Термическая диссоциация СаСl2 → Са2+ + 2Сl-
К(-) Са2+ + 2e- → Са0
А (+) 2Сl- - 2e- → Cl02
Cуммарное уравнение:
СаСl2 → Ca0 + Cl20
3. Рассмотрим электролиз расплава гидроксида калия.
Термическая диссоциация КОН → К+ + ОН-
К(-) К+ + 1e- → К0
А (+) 4ОН- - 4e- → О20 + 2Н2О
Cуммарное уравнение:
4КОН → 4К0 + О20 + 2Н2О
Примеры процессов электролиза растворов электролитов с инертными электродами
В отличие от расплавов в растворе электролита, кроме его ионов, присутствуют молекулы воды. Поэтому при рассмотрении процессов на электродах необходимо учитывать их участие. Электролиз раствора соли, образованной активным металлом, стоящим в ряду напряжений до алюминия и кислотным остатком кислородосодержащей кислоты сводится к электролизу воды. 1. Рассмотрим электролиз водного раствора сульфата магния. MgSO4 – соль, которая образована металлом, стоящим в ряду напряжений до алюминия и кислородсодержащим кислотным остатаком. Уравнение диссоциации: MgSO4 → Mg2+ + SO42- К (-) 2Н2О + 2е- = Н20 + 2ОН- А (+) 2Н2О – 4е- = О20 + 4Н+ Суммарное уравнение: 6Н2О = 2Н20 + 4ОН- + О20 + 4Н+ 2Н2О = 2Н20 + О20 2. Рассмотрим электролиз водного раствора сульфата меди (II). СuSO4 – соль, котороая образована малоактивным металлом и кислородсодержащим кислотным остатком. В данном случае при электролизе получается металл, кислород, а в катодно-анодном пространстве образуется соответствующая кислота. Уравнение диссоциации: CuSO4 → Cu2+ + SO42- К (-) Cu2+ + 2e- = Cu0 А (+) 2Н2О – 4е- = О20 + 4Н+ Суммарное уравнение: 2Cu2+ + 2Н2О = 2Cu0 + О20 + 4Н+ 2CuSO4 + 2Н2О = 2Cu0 + О20 + 2Н2SO4
3. Рассмотрим электролиз водного раствора хлорида кальция. CаCl2 – соль, котороя образована активным металлом и бескислородным кислотным остатком. В данном случае при электролизе образуются водород, галоген, а в катодно – анодном пространстве образуется щелочь. Уравнение диссоциации: CаCl2 → Ca2+ + 2Cl- К (-) 2Н2О + 2е- = Н20 + 2ОН- А (+) 2Сl- – 2е- = Cl20 Суммарное уравнение: 2Н2О + 2Cl- = Cl20 + 2OН- CaCl2 + 2Н2О = Ca(OH)2 + Cl20 + Н20 4. Рассмотрим электролиз водного раствора хлорида меди (II). CuCl2 – соль, которая образована малоактивным металлом и кислотным остатком бескислородной кислоты. В данном случае образуются металл и галоген. Уравнение диссоциации: CuCl2 → Cu2+ + 2Cl- К (-) Cu2+ + 2e- = Cu0 А (+) 2Сl- – 2е- = Cl20 Суммарное уравнение: Cu2+ + 2Cl- = Cu0 + Cl20 CuCl2 = Cu0 + Cl20 5. Рассмотрим процесс электролиза раствора ацетата натрия. СН3СООNa – соль, которая образована активным металлом и кислотным остатком карбоновой кислоты. При электролизе получается водород, щелочь. Уравнение диссоциации: СН3СООNa → СН3СОО - + Na+ К (-) 2Н2О + 2е- = Н20 + 2ОН- А (+) 2CH3COO¯− 2e = C2H6 + 2CO2 Суммарное уравнение: 2Н2О + 2CH3COO¯ = Н20 + 2ОН - + C2H6 + 2CO2 2Н2О + 2CH3COONa = 2NaОH + Н20 + C2H6 + 2CO2 6. Рассмотрим процесс электролиза раствора нитрата никеля. Ni(NO3)2 - соль, которая образована металлом, стоящим в ряду напряжений от Mn до H2 и кислородсодержащим кислотным остатком. В процессе получаем металл, водород, кислород и кислоту. Уравнение диссоциации: Ni(NO3)2 → Ni2+ + 2NO3- К (-) Ni2+ +2e- = Ni0 2Н2О + 2е- = Н20 + 2ОН- A (+) 2H2O – 4e- = O20 + 4H+ Cуммарное уравнение: Ni2+ + 2Н2О + 2H2O = Ni0 + Н20 + 2ОН- + O20 + 4H+ Ni(NO3)2 + 2Н2О = Ni0 +2HNO3 + Н20 + O20 7. Рассмотрим процесс электролиза раствора серной кислоты. Уравнение диссоциации: H2SO4 → 2H+ + SO42- К (-) 2Н+ +2e- = Н20 A (+) 2H2O – 4e- = O20 + 4H+ Cуммарное уравнение: 2Н2О + 4Н+ = 2Н20 + O20 + 4H+ 2H2O = 2Н20 + O20
8. Рассмотрим процесс электролиза раствора гидроксида натрия. В данном случае идет только электролиз воды. Аналогично протекает электролиз растворов H2SO4, NaNO3, K2SO4 и др. Уравнение диссоциации: NaOH → Na+ + OH- К (-) 2H2O + 2e- = H20 + 2OH- A (+) 4OH- – 4e- = O20 + 2H2O Cуммарное уравнение: 4H2O + 4OH- = 2H20 + 4OH- + O20 + 2H2O 2H2O = 2H20 + O20
Примеры процессов электролиза растворов электролитов с растворимыми электродами
Растворимый анод при электролизе сам подвергается окислению (растворению). 1. Рассмотрим процесс электролиза сульфата меди (II) с медным анодом. При электролизе раствора сульфата меди с медным анодом процесс сводится к выделению меди на катоде и постепенному растворению анода, несмотря на природу аниона. Количество сульфата меди в растворе остается неизменным. Уравнение диссоциации: CuSO4 → Cu2+ + SO42- K (-) Cu2+ +2e- → Cu0 A (+) Cu0 - 2e- → Cu2+ переход ионов меди с анода на катод
Примеры заданий по данной теме в вариантах ЕГЭ
В3. (Вар.5)
Установите соответствие между формулой вещества и продуктами электролиза его водного раствора на инертных электродах.
ФОРМУЛА ВЕЩЕСТВА ПРОДУКТЫ ЭЛЕКТРОЛИЗА
A) Al2(SO4)3 1. гидроксид металла, кислота
Б) СsOH 2. металл, галоген
В) Hg(NO3)2 3. металл, кислород
Г) AuBr3 4. водород, галоген 5. водород, кислород 6. металл, кислота, кислород Ход рассуждений: 1. При электролизе Al2(SO4)3 и СsOH на катоде идет восстановление воды до водорода. Исключаем варианты 1, 2, 3 и 6. 2. Для Al2(SO4)3 на аноде окисляется вода до кислорода. Выбираем вариант 5. Для СsOH на аноде окисляется гидроксид ион до кислорода. Выбираем вариант 5. 3. При электролизе Hg(NO3)2 и АuBr3 на катоде идёт восстановление катионов металла. 4. Для Hg(NO3)2 на аноде окисляется вода. Нитрат ионы в растворе связываются с катионами водорода, образуя в анодном пространстве азотную кислоту. Выбираем вариант 6. 5. Для АuBr3 на аноде окисляется анион Br- до Br2. Выбираем вариант 2.
А
Б
В
Г
5
5
6
2
В3. (Вар.1)
Установите соответствие между названием вещества и способом его получения.
НАЗВАНИЕ ВЕЩЕСТВА ПОЛУЧЕНИЕ ЭЛЕКТРОЛИЗОМ А) литий 1) раствора LiF Б) фтор 2) расплава LiF В) серебро 3) раствора MgCl2 Г) магний 4) раствора AgNO3 5) расплава Ag2O 6) расплава MgCl2 Ход рассуждений: 1. Аналогично электролизу расплава хлорида натрия, протекает процесс электролиза расплава фторида лития. Для вариантов А и Б выбираем ответы 2. 2. Серебро возможно восстановить из раствора её соли – нитрата серебра. 3. Из раствора соли магний восстановить нельзя. Выбираем вариант 6 – расплав хлорида магния.
А
Б
В
Г
2
2
4
6
В3. (Вар.9)
Установите соответствие между формулой соли и уравнением процесса, протекающего на катоде при электролизе её водного раствора.
ФОРМУЛА СОЛИ УРАВНЕНИЕ КАТОДНОГО ПРОЦЕССА
А) Al(NO3)3 1) 2H2O – 4e- → O2 + 4H+
Б) CuCl2 2) 2H2O + 2e- → H2 + 2OH-
В) SbCl3 3) Cu2+ + 1e- → Cu+
Г) Cu(NO3)2 4) Sb3+ - 2 e- → Sb5+ 5) Sb3+ + 3e- → Sb0
6) Cu2+ + 2e- → Cu0
Ход рассуждений: 1. На катоде протекают процессы восстановления катионов металлов либо воды. Поэтому сразу исключаем варианты 1 и 4. 2. Для Al(NO3)3: на катоде идёт процесс восстановления воды. Выбираем вариант 2. 3. Для CuCl2: восстанавливаются катионы металла Cu2+. Выбираем вариант 6. 4. Для SbСl3: восстанавливаются катионы металла Sb3+. Выбираем вариант 5. 5. Для Cu(NO3)2: восстанавливаются катионы металла Cu2+. Выбираем вариант 6.
А
Б
В
Г
2
Электрод, на котором происходит восстановление, называется катодом.
Электрод, на котором происходит окисление, - анодом.
Рассмотрим процессы, происходящие при электролизе расплавов солей бескислородных кислот: HCl, HBr, HI, H 2 S (за исключением фтороводородной или плавиковой - HF).
В расплаве такая соль состоит из катионов металла и анионов кислотного остатка.
Например, NaCl = Na + + Cl -
На катоде: Na + + ē = Na образуется металлический натрий (в общем случае - металл, входящий в состав соли)
На аноде: 2Cl - - 2ē = Cl 2 образуется газообразный хлор (в общем случае - галоген, входящий в состав кислотного остатка - кроме фтора - или сера)
Рассмотрим процессы, происходящие при электролизе растворов электролитов.
Процессы, протекающие на электродах, определяются величиной стандартного электродного потенциала и концентрацией электролита (Уравнение Нернста). В школьном курсе не рассматривается зависимость электродного потенциала от концентрации электролита и не используются численные значения величин стандартного электродного потенциала. Ученикам достаточно знать, что в ряду электрохимической напряженности металлов (ряд активности металлов) величина стандартного электродного потенциала пары Me +n /Me:
- увеличивается слева направо
- металлы, стоящие в ряду до водорода, имеют отрицательное значение этой величины
- водород, при восстановлении по реакции 2Н + + 2ē = Н 2 , (т.е. из кислот) имеет нулевое значение стандартного электродного потенциала
- металлы, стоящие в ряду после водорода, имеют положительное значение этой величины
! водород при восстановлении по реакции:
2H 2 O + 2ē = 2OH - + H 2 , (т.е. из воды в нейтральной среде) имеет отрицательное значение стандартного электродного потенциала -0,41
Материал анода может быть растворимым (железо, хром, цинк, медь, серебро и др. металлы) и нерастворимым – инертным – (уголь, графит, золото, платина), поэтому в растворе будут присутствовать ионы, образующиеся при растворении анода:
Ме - nē = Ме +n
Образовавшиеся ионы металла будут присутствовать в растворе электролита и их электрохимическую активность тоже будет нужно учитывать.
Исходя из этого, для процессов, протекающих на катоде, можно определить следующие правила:
1. катион электролита расположен в электрохимическом ряду напряжений металлов до алюминия включительно, идет процесс восстановления воды:
2H 2 O + 2ē = 2OH - + H 2
Катионы металла остаются в растворе, в прикатодном пространстве
2. катион электролита находится между алюминием и водородом, в зависимости от концентрации электролита идет или процесс восстановления воды или процесс восстановления ионов металла. Поскольку концентрация не указывается в задании, записываются оба возможных процесса:
2H 2 O + 2ē = 2OH - + H 2
Ме +n + nē = Ме
3. катион электролита - это ионы водорода, т.е. электролит - кислота. Восстанавливаются ионы водорода:
2Н + + 2ē = Н 2
4. катион электролита находится после водорода, восстанавливаются катионы металла.
Ме +n + nē = Ме
Процесс на аноде зависит от материала анода и природы аниона.
1. Если анод растворяется (например, железо, цинк, медь, серебро), то окисляется металл анода.
Ме - nē = Ме +n
2. Если анод инертный, т.е. не растворяется (графит, золото, платина):
а) При электролизе растворов солей бескислородных кислот (кроме фторидов), идет процесс окисления аниона;
2Cl - - 2ē = Cl 2
2Br - - 2ē = Br 2
2I - - 2ē = I 2
S 2 - - 2ē = S
б) При электролизе растворов щелочей, идет процесс окисления гидроксогруппы ОН - :
4OH - - 4ē = 2H 2 O + O 2
в) При электролизе растворов солей кислородосодержащих кислот: HNO 3 , H 2 SO 4 , H 2 CO 3 , H 3 PO 4 , и фторидов, идет процесс окисления воды.
2H 2 O - 4ē = 4H + + О 2
г) При электролизе ацетатов (солей уксусной или этановой кислоты) окисляется ацетат-ион до этана и оксида углерода (IV) - углекислого газа.
2СН 3 СОО - - 2ē = С 2 Н 6 + 2СО 2
Примеры заданий.
1. Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при электролизе её водного раствора.
ФОРМУЛА СОЛИ
А) NiSO 4
Б) NaClO 4
В) LiCl
Г) RbBr
ПРОДУКТ НА АНОДЕ
1) S 2) SO 2 3) Cl 2 4) O 2 5) H 2 6) Br 2
Решение:
Так как в задании указан инертный анод, мы рассматриваем только изменения, происходящие с кислотными остатками, образующимися при диссоциации солей:
SO 4 2 - кислотный остаток кислородосодержащей кислоты. Идет процесс окисления воды, выделяется кислород. Ответ 4
ClO 4 - кислотный остаток кислородосодержащей кислоты. Идет процесс окисления воды, выделяется кислород. Ответ 4.
Cl - кислотный остаток бескислородной кислоты. Идет процесс окисления самого кислотного остатка. Выделяется хлор. Ответ 3.
Br - кислотный остаток бескислородной кислоты. Идет процесс окисления самого кислотного остатка. Выделяется бром. Ответ 6.
Общий ответ: 4436
2. Установите соответствие между формулой соли и продуктом, образующимся на катоде при электролизе её водного раствора.
ФОРМУЛА СОЛИ
А) Al(NO 3) 3
Б) Hg(NO 3) 2
В) Cu(NO 3) 2
Г) NaNO 3
ПРОДУКТ НА АНОДЕ
1) водород 2) алюминий 3) ртуть 4) медь 5) кислород 6) натрий
Решение:
Так как в задании указан катод, мы рассматриваем только изменения, происходящие с катионами металлов, образующимися при диссоциации солей:
Al 3+ в соответствии с положением алюминия в электрохимическом ряду напряжений металлов (от начала ряда до алюминия включительно) будет идти процесс восстановления воды. Выделяется водород. Ответ 1.
Hg 2+ в соответствии с положением ртути (после водорода) будет идти процесс восстановления ионов ртути. Образуется ртуть. Ответ 3.
Cu 2+ в соответствии с положением меди (после водорода) будет идти процесс восстановления ионов меди. Ответ 4.
Na + в соответствии с положением натрия (от начала ряда до алюминия включительно) будет идти процесс восстановления воды. Ответ 1.
Общий ответ: 1341
Электролиз (греч. elektron - янтарь + lysis - разложение) - химическая реакция, происходящая при прохождении постоянного тока через электролит. Это разложение веществ на их составные части под действием электрического тока.
Процесс электролиза заключается в перемещении катионов (положительно заряженных ионов) к катоду (заряжен отрицательно), и отрицательно заряженных ионов (анионов) к аноду (заряжен положительно).
Итак, анионы и катионы устремляются соответственно к аноду и катоду. Здесь и происходит химическая реакция. Чтобы успешно решать задания по этой теме и писать реакции, необходимо разделять процессы на катоде и аноде. Именно так и будет построена эта статья.
Катод
К катоду притягиваются катионы - положительно заряженные ионы: Na + , K + , Cu 2+ , Fe 3+ , Ag + и т.д.
Чтобы установить, какая реакция идет на катоде, прежде всего, нужно определиться с активностью металла: его положением в электрохимическом ряду напряжений металлов.

Если на катоде появился активный металл (Li, Na, K) то вместо него восстанавливаются молекулы воды, из которых выделяется водород. Если металл средней активности (Cr, Fe, Cd) - на катоде выделяется и водород, и сам металл. Малоактивные металлы выделяются на катоде в чистом виде (Cu, Ag).
Замечу, что границей между металлами активными и средней активности в ряду напряжений считается алюминий. При электролизе на катоде металлы до алюминия (включительно!) не восстанавливаются, вместо них восстанавливаются молекулы воды - выделяется водород.
В случае, если на катод поступают ионы водорода - H + (например при электролизе кислот HCl, H 2 SO 4) восстанавливается водород из молекул кислоты: 2H + - 2e = H 2
Анод
К аноду притягиваются анионы - отрицательно заряженные ионы: SO 4 2- , PO 4 3- , Cl - , Br - , I - , F - , S 2- , CH 3 COO - .

При электролизе кислородсодержащих анионов: SO 4 2- , PO 4 3- - на аноде окисляются не анионы, а молекулы воды, из которых выделяется кислород.
Бескислородные анионы окисляются и выделяют соответствующие галогены. Сульфид-ион при оксилении окислении серу. Исключением является фтор - если он попадает анод, то разряжается молекула воды и выделяется кислород. Фтор - самый электроотрицательный элемент, поэтому и является исключением.
Анионы органических кислот окисляются особым образом: радикал, примыкающий к карбоксильной группе, удваивается, а сама карбоксильная группа (COO) превращается в углекислый газ - CO 2 .
Примеры решения
В процессе тренировки вам могут попадаться металлы, которые пропущены в ряду активности. На этапе обучения вы можете пользоваться расширенным рядом активности металлов.
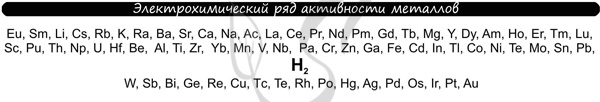
Теперь вы точно будете знать, что выделяется на катоде;-)
Итак, потренируемся. Выясним, что образуется на катоде и аноде при электролизе растворов AgCl, Cu(NO 3) 2 , AlBr 3 , NaF, FeI 2 , CH 3 COOLi.

Иногда в заданиях требуется записать реакцию электролиза. Сообщаю: если вы понимаете, что образуется на катоде, а что на аноде, то написать реакцию не составляет никакого труда. Возьмем, например, электролиз NaCl и запишем реакцию:
NaCl + H 2 O → H 2 + Cl 2 + NaOH
Натрий - активный металл, поэтому на катоде выделяется водород. Анион не содержит кислорода, выделяется галоген - хлор. Мы пишем уравнение, так что не можем заставить натрий испариться бесследно:) Натрий вступает в реакцию с водой, образуется NaOH.
Запишем реакцию электролиза для CuSO 4:
CuSO 4 + H 2 O → Cu + O 2 + H 2 SO 4
Медь относится к малоактивным металлам, поэтому сама в чистом виде выделяется на катоде. Анион кислородсодержащий, поэтому в реакции выделяется кислород. Сульфат-ион никуда не исчезает, он соединяется с водородом воды и превращается в серую кислоту.
Электролиз расплавов
Все, что мы обсуждали до этого момента, касалось электролиза растворов, где растворителем является вода.
Перед промышленной химией стоит важная задача - получить металлы (вещества) в чистом виде. Малоактивные металлы (Ag, Cu) можно легко получать методом электролиза растворов.
Но как быть с активными металлами: Na, K, Li? Ведь при электролизе их растворов они не выделяются на катоде в чистом виде, вместо них восстанавливаются молекулы воды и выделяется водород. Тут нам как раз пригодятся расплавы, которые не содержат воды.

В безводных расплавах реакции записываются еще проще: вещества распадаются на составные части:
AlCl 3 → Al + Cl 2
LiBr → Li + Br 2
© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к
Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при электролизе ее водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА СОЛИ | ПРОДУКТ НА АНОДЕ | |
| A | Б | В | Г |
Решение.
При электролизе водных растворов солей, щелочей и кислот на инертном аноде:
Разряжается вода и выделяется кислород, если это соль кислородсодержащей кислоты или соль фтороводородной кислоты;
Разряжаются гидроксид-ионы и выделяется кислород, если это щелочь;
Разряжается кислотный остаток, входящий в состав соли, и выделяется соответствующее простое вещество, если это соль бескислородной кислоты(кроме ).
По особому происходит процесс электролиза солей карбоновых кислот.
Ответ: 3534.
Ответ: 3534
Источник: Яндекс: Тренировочная работа ЕГЭ по химии. Вариант 1.
Установите соответствие между формулой вещества и продуктом, образующимся на катоде при электролизе его водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | ПРОДУКТ ЭЛЕКТРОЛИЗА, ОБРАЗУЮЩИЙСЯ НА КАТОДЕ |
|
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
| A | Б | В | Г |
Решение.
При электролизе водных растворов солей на катоде выделяется:
Водород, если это соль металла, стоящего в ряду напряжений металлов левее алюминия;
Металл, если это соль металла, стоящего в ряду напряжений металлов правее водорода;
Металл и водород, если это соль металла, стоящего в ряду напряжений металлов между алюминием и водородом.
Ответ: 3511.
Ответ: 3511
Источник: Яндекс: Тренировочная работа ЕГЭ по химии. Вариант 2.
Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при электролизе её водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА СОЛИ | ПРОДУКТ НА АНОДЕ | |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
| A | Б | В | Г |
Решение.
При электролизе водных растворов солей кислородсодержащих кислот и фторидов окисляется кислород из воды, поэтому на аноде выделяется кислород. При электролизе водных растворов бескислородных кислот идет окисление кислотного остатка.
Ответ: 4436.
Ответ: 4436
Установите соответствие между формулой вещества и продуктом, который образуется на инертном аноде в результате электролиза водного раствора этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | ПРОДУКТ НА АНОДЕ |
2) оксид серы(IV) 3) оксид углерода(IV) 5) кислород 6) оксид азота(IV) |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
| A | Б | В | Г |








 Что такое троицкая родительская суббота и что нельзя делать в этот день Можно ли работать в троицкую родительскую субботу
Что такое троицкая родительская суббота и что нельзя делать в этот день Можно ли работать в троицкую родительскую субботу Два рецепта, как заваривать морошку от кашля
Два рецепта, как заваривать морошку от кашля Положительная социально-психологическая атмосфера коллектива, как основа полноценного развития дошкольника
Положительная социально-психологическая атмосфера коллектива, как основа полноценного развития дошкольника Правило четное и нечетное
Правило четное и нечетное